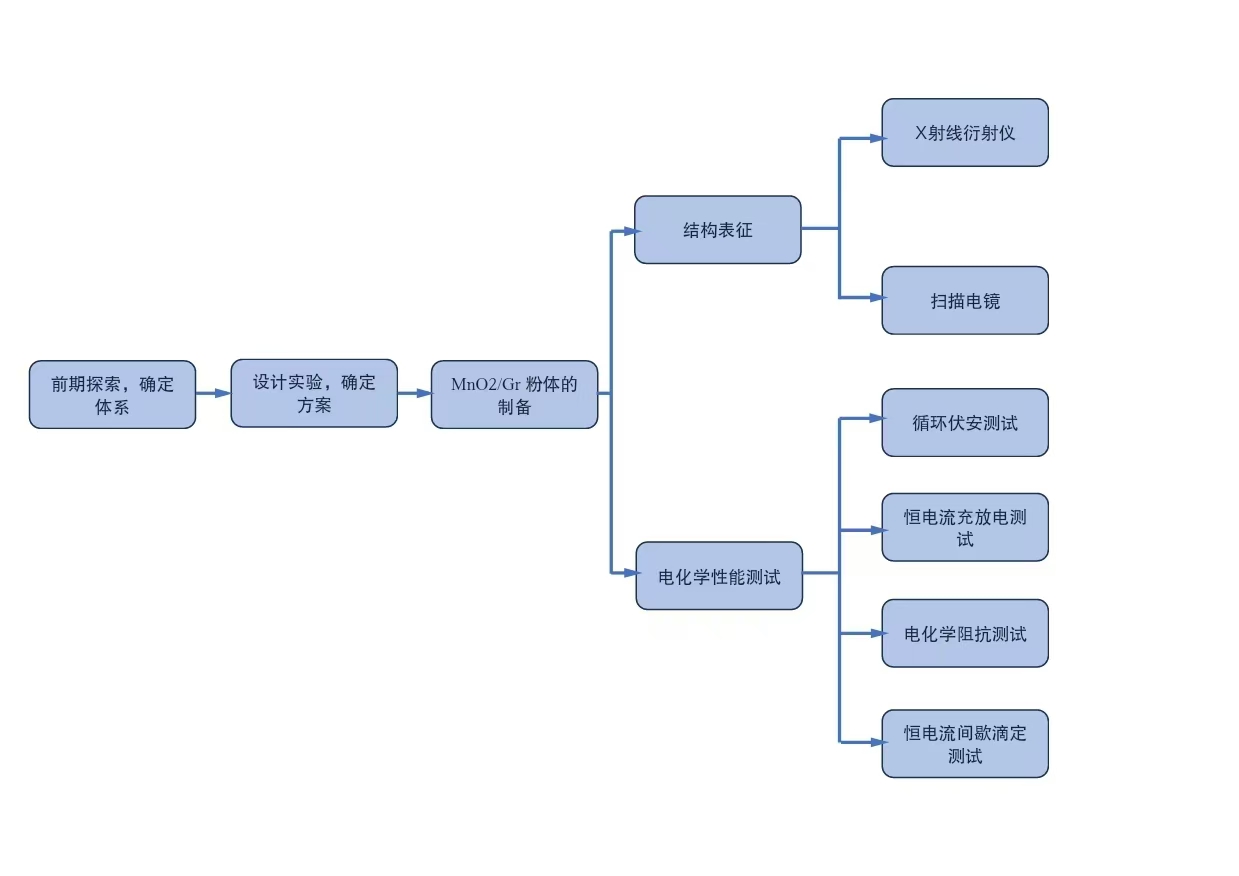
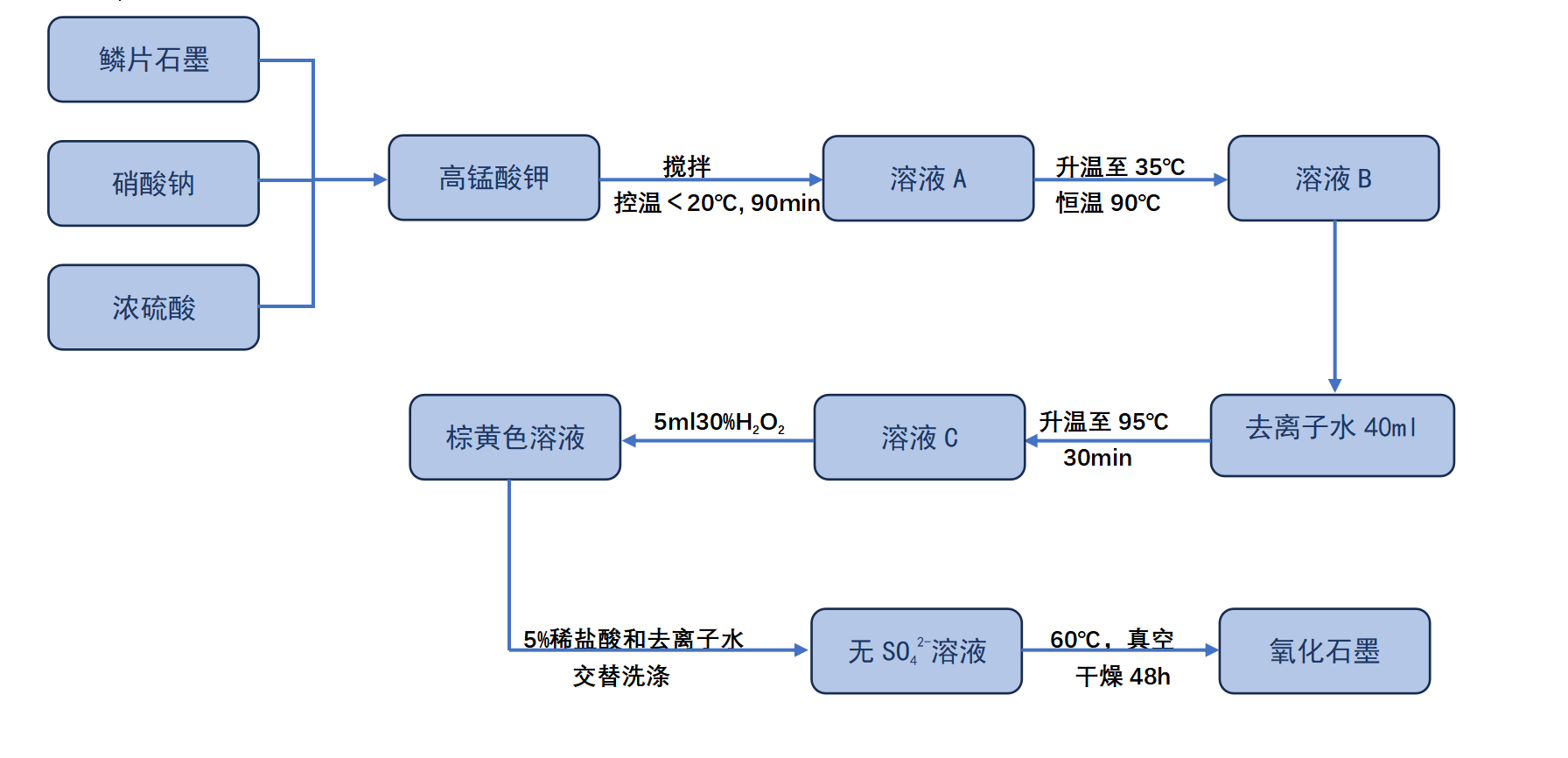
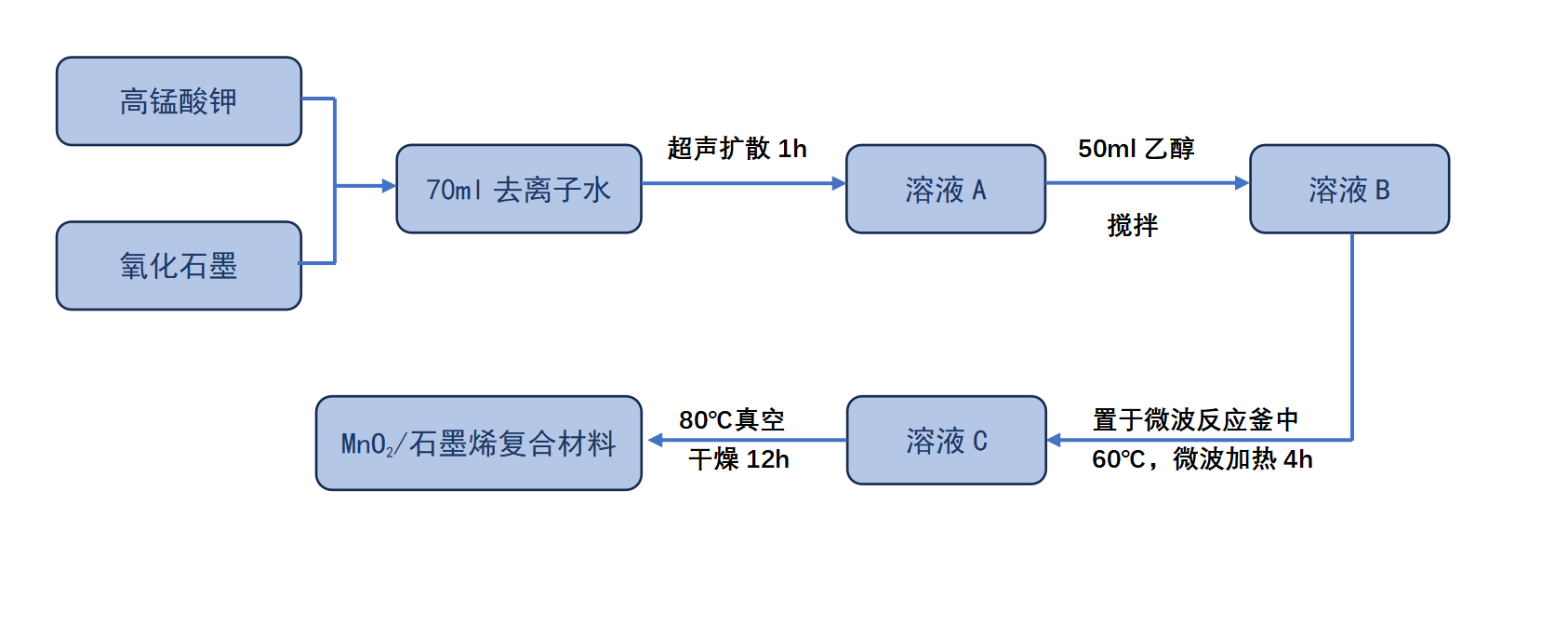
AZIBs的发展历史悠久,可追溯至十九世纪后期,1986年,Yamamoto等人首次提出了以ZnSO4作为电解质的Zn-MnO2电池体系[1]。2011年,Kang等人提出“Zn-ion battery”的概念,将MnO2作为正极组装成纽扣电池,可以实现可逆的Zn2+插入/提取[2]。从那时起,研究者们致力于探索各种AZIBs体系,研发包括锌-钒基电池、锌-钼基电池、锌-醌电池和锌-普鲁士蓝类似物电池等,这些电池即使在弱酸性电解质环境下也可以实现稳定的循环。这些突破性进展极大地推动了可充电锌基电池(RZBs)的发展,同时,为LIBs提供了一种很好的替代品,为新一代能源储存技术提供了新的机遇。
AZIBs初期的储能机理被认为是Zn2+在正极材料中可逆地嵌入/脱出。Kang等人首次提出在电池不同的充放电阶段,可以在α-MnO2正极中实现Zn2+的可逆嵌入/脱出,并发现Zn2+插入α-MnO2后会生成ZnMn2O4,这一储能机制与传统的碱性锌锰电池所依赖的两步储能机制截然不同。通过原位XRD技术的应用,Kim团队探究了α-MnO2纳米棒在储锌方面的反应机理[3]。研究发现,Zn2+能够可逆地在纳米棒中进行嵌入和脱出过程,这一发现与先前的研究结果相吻合。此外,在连续的充放电过程中,其晶面对应的晶格间距会随之改变,这可以缓解材料的体积膨胀问题,从而增强了α-MnO2的结构稳定性[3]。He等人在随后的研究中也发现,即使更换不同种类的β-MnO2、γ-MnO2、λ-MnO2、δ-MnO2正极材料,同样会发生Zn2+的嵌入/脱出反应。α-MnO2具有相对大且稳定的(2×2)隧道,因此成为锌离子电池正极材料的研究热点。然而,结构不稳定、导电性差等导致α-MnO2在循环过程中容量衰减快、倍率性能差,也是一个具有挑战性的问题[4]。Li等通过水热法合成了一种新型正极材料α-MnO2@In2O3。在α-MnO2纳米管上均匀涂覆In2O3后,增加了其电导率,显著改善了材料的循环稳定性和倍率性能。α-MnO2@In2O3在100mA·g-1的电流密度下经过100次循环后表现出425mAh·g-1的高比容量,且在3A·g-1的高电流密度下长时间循环3000次后比容量仍能保持为115.5mAh·g-1[5]。而近期,Chen团队认为,α-MnO2在充电过程会发生电沉积的副反应影响电化学性能,该副反应的过程是电解质Mn离子不可逆转化为电化学钝化物,使得电荷转移阻抗增大,从而触发电池性能退化的原因。该团队将表面缺陷有限的石墨纳米片(GNS)加入到α-MnO2电极中,阻碍了Mn的吸附速率,从而有效地抑制了电沉积反应。由此制备的无粘结剂α-MnO2薄膜电极在超过600次循环中可以实现接近100%容量的单电子可逆反应,平均库伦效率约为99.8%。β-MnO2在热力学上是MnO2各晶型中最稳定的相,但与其他隧道型MnO2相比,β-MnO2的(1×1)隧道是最窄的(2.3Å),因此Zn2+在β-MnO2中的嵌入有些困难,从而在锌离子电池中表现出较差的电化学活性[6]。2017年,Kim课题组首次通过简单的微波辅助水热法合成了具有暴露(101)面的隧道型β-MnO2纳米棒,用作ZIBs的高性能正极材料。β-MnO2中Zn2+的储存机制被认为是Zn2+嵌入和转化的复合反应:在初始循环中,Zn2+嵌入到β-MnO2中;在第30次循环后,发生从β-MnO2到ZnMn2O4的相变以及ZnSO4·5Zn(OH)2·5H2O的沉淀;随后,可逆的Zn2+嵌入/脱出过程将在形成的ZnMn2O4结构中进行。暴露(101)面的β-MnO2纳米棒表现出在100mA·g-1下,放电容量为270mAh·g-1,在200mA·g-1下,经过200次循环,容量保持率为75%。这一研究表明通过控制β-MnO2的形态或暴露表面,可以极大提高β-MnO2晶体的电化学性能[7]。Chen课题组通过在3MZn(CF3SO3)2电解液中添加0.1MMn(CF3SO-)2的高性能可充电Zn-MnO2电池。在初始放电期间隧道型β-MnO2转变为层状相Zn0.5MnO2·nH2O,随后Zn2+在层状结构中可逆地嵌入/脱出。同时,预先添加Mn(CF3SO3)2实现了Mn2+溶解和再氧化之间的平衡,并在正极表面上形成均匀的多孔MnOx纳米片层,有助于保持电极完整性。Mn(CF3SO3)2添加剂显著提高了Zn-MnO2电池的循环稳定性:在2000次循环中容量保持率为94%;软包Zn-MnO2电池经过50次循环后,其可逆容量为1550mAh,总能量密度为75.2Wh·kg-1[8]。这种方法是由Liu课题组首先提出来的,他们在2MZnSO4电解液中添加0.1MMnSO4来抑制α-MnO2中Mn的溶解[9]。最近,Kang等人采用水热法制备了β-MnO2纳米棒,并通过对充放电过程的研究,提出了质子转换和Mn2+溶解/沉积机理。β-MnO2与质子反应生成MnOOH,在第一次放电过程中MnOOH转化为Mn2+;在第一次充电时,MnOOH和Mn2+转换并沉积为ε-MnO2。在之后的循环中则发生ε-MnO2和MnOOH或Mn2+之间的两相转化反应,并伴随质子转换和Mn2+的溶解/沉积。Zn//β-MnO2在0.1A·g-1时可提供355mAh·g-1的高容量,在0.2A·g-1时经1000次循环后,在低电流密度下也表现出高稳定性,容量保持为110mAh·g-1。δ-MnO2相比于MnO2隧道结构,具有典型层状结构的δ-MnO2理论上更有利于Zn2+的嵌入,因此也是极具吸引力的锌离子电池正极材料[10]。
Khamsanga等人首次报道生长在石墨薄片上具有层状结构的δ-MnO2正极,其能够快速实现Zn2+的嵌入和脱出过程。放电时,在锌负极一侧会发生Zn的溶解,电解质中的Zn2+会嵌入到δ-MnO2的层间[11]。掺杂是提高材料本体导电性的常规方法。Shao等人首先发现Co修饰δ-MnO2具有较好的自恢复能力通过连续催化活性锰化合物的电化学沉积,正极中钴元素能够有效地自我回收。在优化的条件下,获得了超过500mAh g-1的高比容量,以及良好的循环性能,5000次循环的保留率为63%。有了这种钴促进沉积效应,在电解液中添加较低浓度Mn2+(0.02M)的电池仍能保持良好的容量保持。此外,表面涂层可以抑制Mn2+离子的溶解[12]。Mai等人设计了一种石墨烯卷涂的α-MnO2用于AZIBs的正极。研究表明,Zn2+优先被嵌入到α-MnO2的框架中,形成层状相。当Zn2+连续嵌入正极材料后,储存空间变小,这时Zn2+通过两步插层机制嵌入到α-MnO2的通道中。Mai等人比较了石墨烯包覆α-MnO2纳米线(MGS)和原始α-MnO2纳米线的电化学储锌性能。石墨烯降低正极材料的溶解和大大提高了导电性[13]。
参考文献:
[1] Yamamoto T, Shoji T. Rechargeable Zn|ZnSO4|MnO2-type cells [J]. Inorganica Chimica Acta, 1986, 117(2):L27-L28.
[2] XU C J, LI B H, DU H D, et al. Energetic zinc ion chemistry: The rechargeable zinc ion battery[J]. Angewandte Chemie, International Edition, 2012, 51(4): 933-935.
[3] ALFARUQI M H, GIM J, KIM S, et al. Enhanced reversible divalent zinc storage in a structurally stable a-MnO2 nanorod electrode[J]. Journal of Power Sources, 2015, 288: 320-327.
[4] MAO M, WU X X, HU Y, et al. Charge storage mechanism of MOF-derived Mn2O3 as high performance cathode of aqueous zinc-ion batteries[J]. Journal of Energy Chemistry, 2021, 52: 277- 283.
[5] Gou L, Xue D, Mou K L, et al. Alpha-MnO2@In2O3 Nanotubes as CathodeMaterial for Aqueous Rechargeable Zn-Ion Battery with High ElectrochemicalPerformance[J]. Journal of the Electrochemical Society,2019,166(14):A3362-A3368.
[6] Liang R L, Fu J, Deng Y P, et al. Parasitic Electrodeposition in Zn-MnO2 Batteries and its Suppression for Prolonged Cyclability[J]. Energy Storage Materials, 2021,36:478-4.
[7] Islam S, Alfaruqi M H, Mathew V, et al. Facile Synthesis and the Exploration of the Zinc Storage Mechanism of Beta-MnO2 Nanorods with Exposed (101) Planes as a Novel Cathode Material for High Performance Eco-Friendly Zinc-Ion Batteries[J]. Journal of Materials Chemistry A, 2017,5(44):23299-2330
[8] Zhang N, Cheng F Y, Liu J X, et al. Rechargeable Aqueous Zinc-Manganese Dioxide Batteries with High Energy and Power Densities[J]. Nature Communication, 2017,8:405.
[9] Pan H L, Shao Y Y, Yan P F, et al. Reversible Aqueous Zinc/Manganese Oxide Energy Storage from Conversion Reactions[J]. Nature Energy,2016,1:1603.
[10] Liu W B, Zhang X Y, Huang Y F, et al. beta-MnO2 with Proton ConversionMechanism in Rechargeable Zinc Ion Battery[J]. Journal of Energy Chemistry,2021,56:365-373.
[11]KHAMSANGA S, PORNPRASERTSUK R, YONEZAWA T, et al. 0-MnO2 nanoflower/graphite cathode for rechargeable aqueous zinc ion batteries[J]. Scientific Reports, 2019, 9: 8441.
[12] Zhong Y, Xu X, Veder J P, et al. Self-Recovery Chemistry and Cobalt-Catalyzed Electrochemical Deposition of Cathode for Boosting Performance of Aqueous Zinc-Ion Batteries [J]. iScience, 2020, 23(3):100943.
[13] Wu B K, Zhang G B, Yan M Y, et al. Graphene Scroll-Coated Alpha-MnO2Nanowires as High-Performance Cathode Materials for Aqeous Zn-Ion Battery[J]. Small, 2018,14(13):1703850.