1. 天然多糖基水凝胶研究现状及动态
多糖是与糖苷键相连的碳水化合物分子的长链,天然多糖在自然界中分布广泛,一些天然聚合物还具有抗菌的特性[1, 2]。因此,多糖聚合物如明胶、普鲁兰多糖和壳聚糖等生物高分子材料已被广泛用于制备伤口敷料,由于其无毒、抗菌、生物相容、止血和非免疫原性等特性,在生物医学领域得到极大的应用。大多数这些聚合物以泡沫、薄膜、海绵和纤维的形式用于药物载体装置、皮肤组织支架和伤口敷料中。目前,使用天然聚合物合成水凝胶伤口敷料时,高保水能力使其成为制备伤口敷料的最佳选择,它们在伤口中提供潮湿环境并去除多余的伤口液体,从而加速伤口愈合[3]。
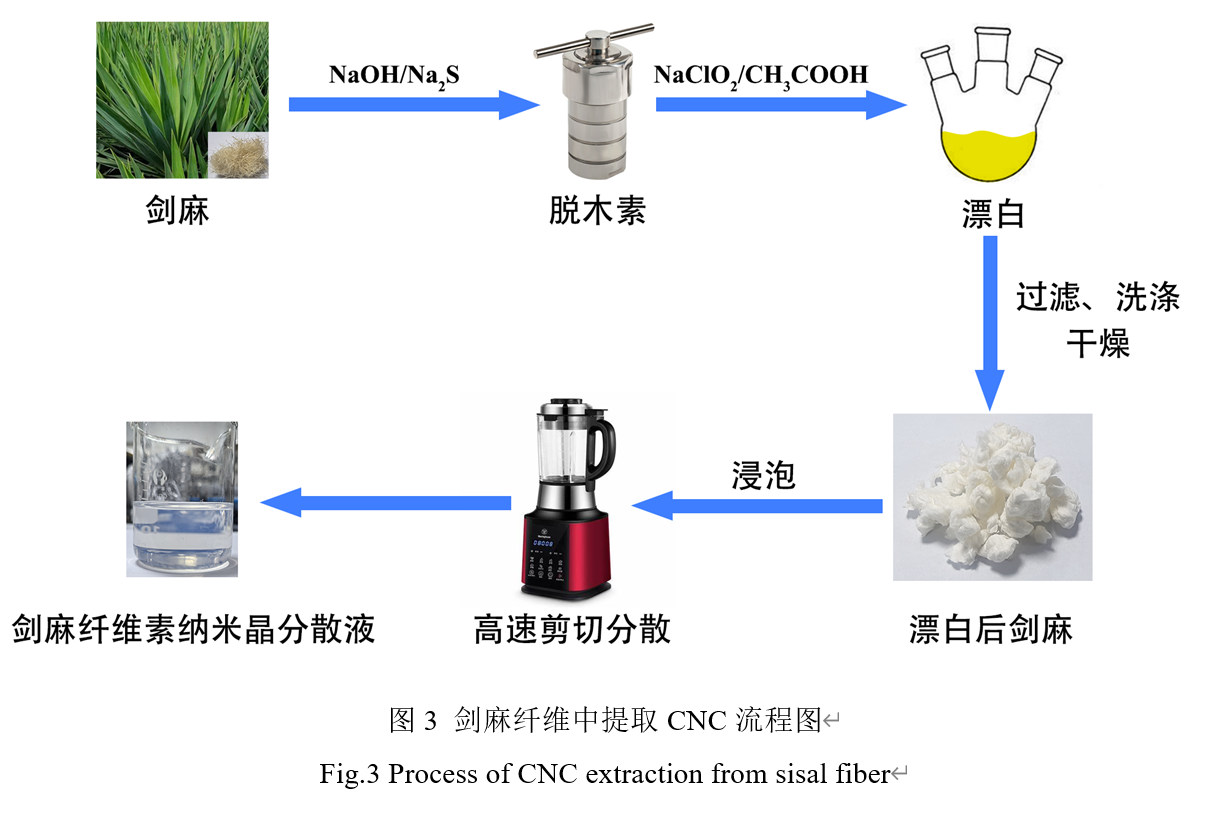
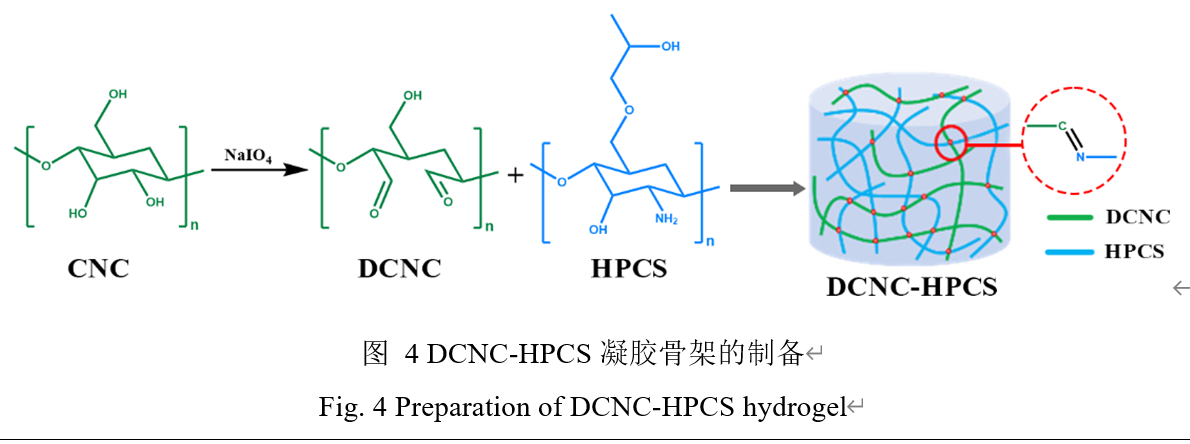
纤维素是地球上最丰富的天然聚合物。纤维素存在于植物中,大约15-30%在原细胞壁中,超过40%在次级细胞壁中。次生细胞壁是最厚的层,对植物的机械性能也是最重要的[4]。天然来源的纤维素具有可回收性、可调表面特性、毒性风险小、生物降解性、生物相容性[5]。纤维素基水凝胶在除了生物医学领域最常见外,还包括生物传感和水净化。常见纳米纤维的三种类型,即细菌纳米纤维素,纤维素纳米晶和纤维素纳米纤维。细菌纳米纤维素用于抗菌伤口愈合,可以安全有效地改善伤口愈合。纤维素纳米晶是具有可调表面化学性质的优良生物材料。最近,一些研究集中在纤维素纳米晶体通过酯化[6]、氧化[7]、氨基甲酸酯[8]、酰胺化[9]、醚化[10]的改性上。高碘酸盐的氧化导致纤维素碳原子上的C2和C3碳键裂解和醛官能团的形成,因此,二醛纤维素纳米晶可以与壳聚糖及其衍生物或明胶中的游离氨基发生反应,这种类型的反应被称为席夫碱反应[11]。水凝胶是一种交联聚合物网络,具有很高的保水能力,广泛应用于生物医学领域。由于增加的柔韧性和缠结倾向,CNF有利于形成机械稳定的水凝胶,CNC水凝胶易于降解,膨胀率过高和机械不稳定。在生物医学工程的情况下,膨胀和脱胀动力学以及可控的降解是细胞生长和组织再生的主要因素[5]。
壳聚糖是一种天然多糖,主要来源于昆虫(角质层)和甲壳类动物(如蟹、虾和龙虾等)[12]。天然多糖甲壳素经过部分脱乙酰化以提供壳聚糖,壳聚糖是最常用的大分子之一[13, 14]。除了抗菌特性外,它还具有可生物降解和生物相容性[13]。然而,由于壳聚糖的水溶性差,壳聚糖的应用在一定程度上受到限制。羟丙基壳聚糖(羟丙基脱乙酰壳聚糖,HPCS)通过引入一定量的羟丙基来提高壳聚糖在水中的溶解度。与壳聚糖相比,它具有更好的吸湿性、保水性以及交联性能[15]。这些特性使羟丙基壳聚糖成为理想的止血材料,并有望作为伤口愈合促进剂。为制备生物基材料并赋予其实用性能,将包括木聚糖,纤维素和壳聚糖在内的一些多糖改性以期一方面可以保留纤维素基水凝胶的原本的优良特性, 另一方面可以赋予其本身所不具备的优点, 以拓宽其应用价值。
Qiu[16]等人以聚乙烯醇和羟丙基壳聚糖为底物制备了双交联网络水凝胶,使用 HPCS 和 PVA 作为底物来制造水凝胶,并使用硼砂和 OSA 作为交联剂,具有动态亚胺和硼酸盐键合双交联网络的水凝胶是通过简单的混合方法制备的,该双交联网络使水凝胶具有出色的自修复和机械性能,对药物体外释放速率、生物毒性以及水凝胶的抗菌和降解特性进行评估,发现其具有潜在的医疗应用价值。Liu[17]等人通过基于丝素蛋白肽接枝羟丙基壳聚糖 (HPCS-g-SFP) 和氧化微晶纤维素 (OMCC) 通过席夫碱键开发了一种可注射HMSC水凝胶,HPCS-g-SFP 共聚物对氢羟基自由基和 1,1-二苯基-2-三硝基苯肼自由基 (DPPH) 表现出高效的自由基清除能力,并将四甲基吡嗪 (TMP) 封装到 HMSC 水凝胶中,得到负载 TMP 的 HMSC 水凝胶,负载 TMP 的 HMSC 水凝胶具有能保留95%细胞活性并可促进伤口快速愈合,同时防止疤痕形成,具有促进无疤痕伤口愈合的潜力。Peng[18]等人希夫碱反应以及羟丙基壳聚糖 (HCS)、ε-聚-l-赖氨酸 (EPL) 和 2,3,4-三羟基苯甲醛 (TBA) 之间的氢键,以及Fe3+和邻苯三酚之间可逆配位形成的多重交联,通过一锅法成功制备了一系列可注射复合水凝胶,并该水凝胶表现出优异的物理化学特性,包括注射性、自愈性、保水性和粘附性,能够长时间填充不规则的伤口,为伤口愈合提供合适的潮湿环境,该水凝胶还具有优异的止血性能可以快速止血,避免急性创伤中大量失血的严重后遗症,该简单的合成多功能注射止血抗菌水凝胶可以在未愈合、感染伤口的生理环境中杀死细菌并促进愈合,并用于临床治疗的潜力。Liu[19]等人通过乙酰乙酸纤维素 (CAA)、羟丙基壳聚糖 (HPCS) 和氨基改性纤维素纳米晶体制备了一种具有 pH 响应特性和优异的稳定性水凝胶,在酸性条件下通过烯胺键交换表现出自修复行为,此外,对成纤维细胞 L929 细胞的 CCK-8 细胞毒性研究表明 CNC 增强水凝胶具有良好的生物相容性,结果表明,该CNC 增强注射和自修复水凝胶在生物医学领域具有巨大的应用潜力。
2. 天然黑色素纳米粒光热治疗研究现状及动态
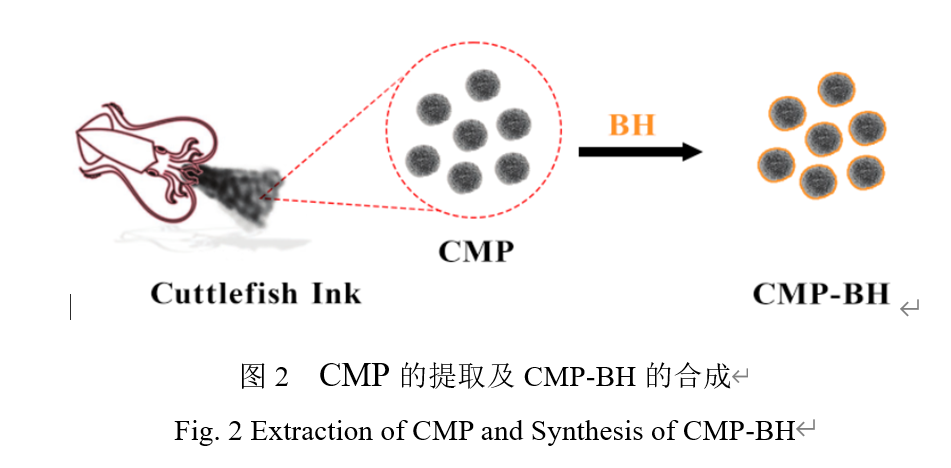
黑色素类生物聚合物广泛存在于皮肤、头发、眼睛虹膜、脑髓质等人体组织和器官中,广泛应用于诊断、生物传感器和组织工程等生物医学领域,表明它们具有良好的生物相容性[20, 21]。其中,从墨鱼墨囊中提取的黑色素纳米颗粒(CMP)具有丰富的黑色素成分从而具有优异的光热特性,已用于肿瘤治疗和活性氧清除[22]。CMP的表面具有一定的儿茶酚结构,这不仅赋予了它们高性能的组织粘附性能,而且还允许它们通过分子间氢键与其他材料络合[23]。此外,CMP表面有丰富的芳香环,可以通过π-π堆积或氢键结合在其表面负载化学药物,从而赋予CMP负载药物的能力。
Fan [24]等人合成了水溶性黑色素纳米颗粒,并通过黑色素与索拉非尼芳香族结构之间的强结合相互作用将索拉非尼负载在其表面,开发了一种基于黑色素的治疗诊断学平台,用于黑色素瘤和肿瘤药物递送的多模态成像。由于天然的黑色中含有具有丰富胺基[25],Zhang[26]等人通过血卟啉的羧基与黑色素纳米颗粒的胺基反应制备了血卟啉-黑色素纳米偶联物 (HMNCs),生物启发的 HMNC 能够实现高生物相容性、US 触发的声动力学疗法(SDT)和 NIR 激光诱导的 PTT,与单独使用 SDT 或 PTT 相比,联合 SDT-PTT 在体外对癌细胞的治疗效果要高得多,通过小鼠静脉注射 HMNCs 实验发现,HMNCs 可以在肿瘤区域内积累,为肿瘤光声 (PA) 和热成像提供高对比度,并与单独使用 SDT 或 PTT 相比,通过协同 SDT-PTT 高度抑制肿瘤生长,同时未观察到明显的副作用,表明该受生物启发的 HMNC 可以作为肿瘤治疗诊断学的优秀 SDT-PTT 纳米制剂。Li[27]等人基于己二酰肼改性透明质酸、苯甲醛基团功能化聚乙二醇)-共聚(癸二酸甘油酯)和墨鱼黑色素纳米颗粒开发了一种可注射胶粘剂自修复光热双动态席夫碱网络水凝胶,它具有优秀的组织粘附性、拉伸性和自愈特性,使它们能够适应运动伤口的频繁运动,该胶粘剂自修复光热水凝胶可以适应运动伤口的频繁运动,并且可以改善感染并促进正常和感染运动伤口的愈合,这表明它们在临床运动伤口治疗中具有巨大潜力。Caldas[28]等人通过天然黑色素纳米颗粒(MNP)负载阿霉素(DOX)制成的新型药物递送纳米平台,在不使用无毒溶剂的情况下具有 99% 的阿霉素 (Dox) 掺入效率,48小时后,在光热刺激下观察到约 23% 的药物持续释放,而在没有刺激的情况下为 15%,并且当将载有 Dox (Dox-MNP) 的天然 MNP 与 SaOs-2 细胞接触并同时接受 NIR 光时,观察到癌细胞在 48 小时内减少了 93%,表明了化疗和光疗之间的协同效果,这是首次从棕褐色中提取的天然 MNP 作为化疗光热剂在骨肉瘤细胞系上进行测试,表明这些 NP 是一种有效、经济高效、可重复、无毒的纳米平台,有潜力用于化疗和光热协同治疗骨肉瘤,促进靶向递送、高局部浓度和降低全身毒性。
参考文献
[1] Junter G-A, Thébault P, Lebrun L. Polysaccharide-based antibiofilm surfaces[J]. Acta Biomaterialia, 2016, 30: 13-25.
[2] Venkatesan J, Lowe B, Anil S, et al. Seaweed polysaccharides and their potential biomedical applications[J]. Starch - Stärke, 2015, 67(5-6): 381-390.
[3] Elangwe CN, Morozkina SN, Olekhnovich RO, et al. Pullulan-Based Hydrogels in Wound Healing and Skin Tissue Engineering Applications: A Review[J]. International Journal of Molecular Sciences, 2023, 24(5): 4962.
[4] Nascimento DM, Nunes YL, Figueirêdo MCB, et al. Nanocellulose nanocomposite hydrogels: technological and environmental issues[J]. Green Chemistry, 2018, 20(11): 2428-2448.
[5] Shojaeiarani J, Bajwa D, Shirzadifar A. A review on cellulose nanocrystals as promising biocompounds for the synthesis of nanocomposite hydrogels[J]. Carbohydrate Polymers, 2019, 216: 247-259.
[6] Ávila Ramírez JA, Fortunati E, Kenny JM, et al. Simple citric acid-catalyzed surface esterification of cellulose nanocrystals[J]. Carbohydrate Polymers, 2017, 157: 1358-1364.
[7] Wang L, Du Y, Yuan Y, et al. Mussel-inspired fabrication of konjac glucomannan/microcrystalline cellulose intelligent hydrogel with pH-responsive sustained release behavior[J]. International Journal of Biological Macromolecules, 2018, 113: 285-293.
[8] Willberg-Keyriläinen P, Hiltunen J, Ropponen J. Production of cellulose carbamate using urea-based deep eutectic solvents[J]. Cellulose, 2018, 25(1): 195-204.
[9] Zubik K, Singhsa P, Wang Y, et al. Thermo-Responsive Poly(N-Isopropylacrylamide)-Cellulose Nanocrystals Hybrid Hydrogels for Wound Dressing[J]. Polymers, 2017, 9(4): 119.
[10] Li B, Xu C, Yu J, et al. One-pot cellulose etherification and self-crosslinking via a mild hydroxyl–yne click reaction in a homogeneous system[J]. Green Chemistry, 2023, 25(7): 2608-2619.
[11] Elangwe CN, Morozkina SN, Olekhnovich RO, et al. A Review on Chitosan and Cellulose Hydrogels for Wound Dressings[J]. Polymers, 2022, 14(23): 5163.
[12] Bai Q, Gao Q, Hu F, et al. Chitosan and hyaluronic-based hydrogels could promote the infected wound healing[J]. International Journal of Biological Macromolecules, 2023, 232: 123271.
[13] Abdel-Gawad R, Osman R, Awad GaS, et al. Wound healing potential of silver nanoparticles embedded in optimized bio-inspired hybridized chitosan soft and dry hydrogel[J]. Carbohydrate Polymers, 2024, 324: 121526.
[14] Yang Y, Ma Y, Wang J, et al. Chitosan-based mussel-inspired hydrogel for rapid self-healing and high adhesion of tissue adhesion and wound dressings[J]. Carbohydrate Polymers, 2023, 316: 121083.
[15] Zhong Y, Seidi F, Wang Y, et al. Injectable chitosan hydrogels tailored with antibacterial and antioxidant dual functions for regenerative wound healing[J]. Carbohydrate Polymers, 2022, 298: 120103.
[16] Qiu J, Lan J, Xiang Y, et al. An injectable, self-healable, and antimicrobial hydroxypropyl chitosan/poly(vinyl alcohol) hydrogel for drug delivery systems[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2024, 698: 134587.
[17] Liu S, Zhao Y, Wei H, et al. Injectable hydrogels based on silk fibroin peptide grafted hydroxypropyl chitosan and oxidized microcrystalline cellulose for scarless wound healing[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2022, 647: 129062.
[18] Peng S, Niu S, Gao Q, et al. Hydroxypropyl chitosan/ε-poly-l-lysine based injectable and self-healing hydrogels with antimicrobial and hemostatic activity for wound repair[J]. Carbohydrate Polymers, 2024, 337: 122135.
[19] Liu H, Li C, Wang B, et al. Self-healing and injectable polysaccharide hydrogels with tunable mechanical properties[J]. Cellulose, 2018, 25(1): 559-571.
[20] Mrówczyński R, Markiewicz R, Liebscher J. Chemistry of polydopamine analogues[J]. Polymer International, 2016, 65(11): 1288-1299.
[21] Liu Y, Ai K, Liu J, et al. Dopamine-Melanin Colloidal Nanospheres: An Efficient Near-Infrared Photothermal Therapeutic Agent for In Vivo Cancer Therapy[J]. Advanced Materials, 2013, 25(9): 1353-1359.
[22] Deng R-H, Zou M-Z, Zheng D, et al. Nanoparticles from Cuttlefish Ink Inhibit Tumor Growth by Synergizing Immunotherapy and Photothermal Therapy[J]. ACS Nano, 2019, 13(8): 8618-8629.
[23] Zeng Q, Peng Q, Wang F, et al. Tailoring Food Biopolymers into Biogels for Regenerative Wound Healing and Versatile Skin Bioelectronics[J]. Nano-Micro Letters, 2023, 15(1): 153.
[24] Fan Q, Cheng K, Hu X, et al. Transferring Biomarker into Molecular Probe: Melanin Nanoparticle as a Naturally Active Platform for Multimodality Imaging[J]. Journal of the American Chemical Society, 2014, 136(43): 15185-15194.
[25] Wang Z, Yu N, Yu W, et al. In situ growth of Au nanoparticles on natural melanin as biocompatible and multifunctional nanoagent for efficient tumor theranostics[J]. Journal of Materials Chemistry B, 2019, 7(1): 133-142.
[26] Zhang J, Shi C, Shan F, et al. From biology to biology: Hematoporphyrin-melanin nanoconjugates with synergistic sonodynamic-photothermal effects on malignant tumors[J]. Chemical Engineering Journal, 2021, 408: 127282.
[27] Jiang Q, Luo Z, Men Y, et al. Red blood cell membrane-camouflaged melanin nanoparticles for enhanced photothermal therapy[J]. Biomaterials, 2017, 143: 29-45.
[28] Caldas M, Barbosa AI, Bhattacharya M, et al. Natural melanin nanoparticles (MNPs) extracted from Sepia officinalis: A cost-effective, chemo-photothermal, synergistic nanoplatform for osteosarcoma treatment[J]. Colloids and Surfaces B: Biointerfaces, 2024, 239: 113937.

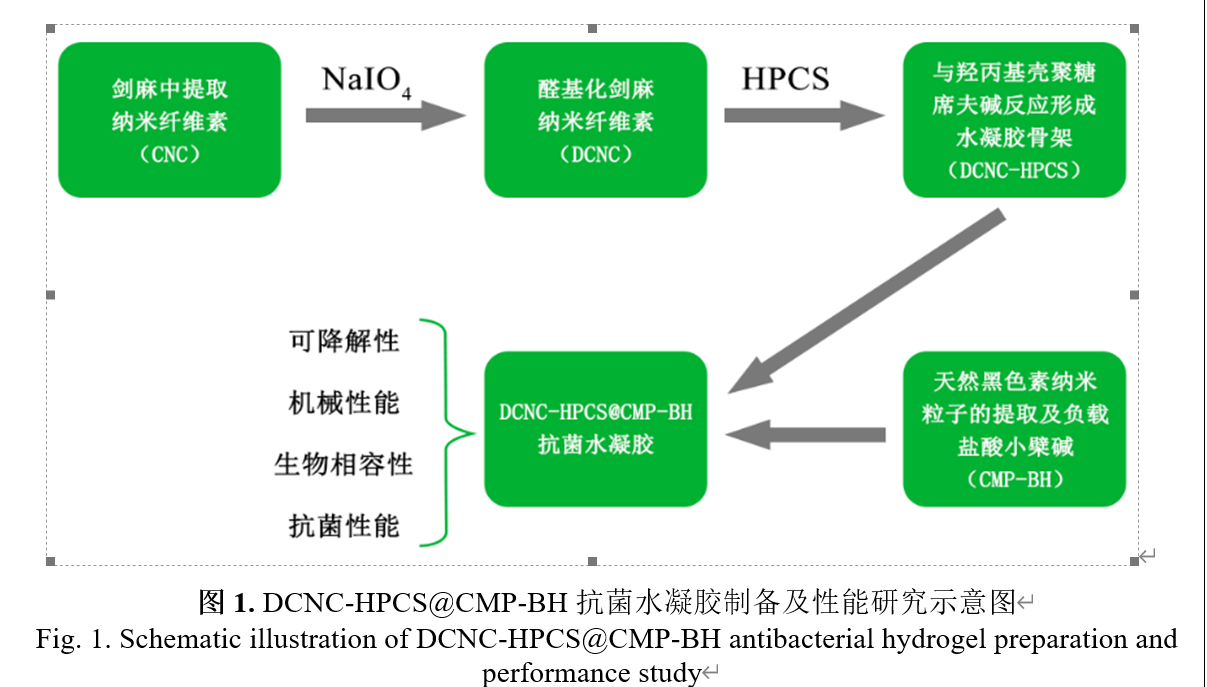 1. CMP-BH纳米粒子的制备
1. CMP-BH纳米粒子的制备