国、内外研究现状和发展动态
植硅体是高等植物通过吸收地下水中可溶性二氧化硅沉淀于植物细胞内或细胞壁之间而形成的固体二氧化硅矿物[1]。植硅体在植物腐烂、分解、搬运、埋藏过程中具有很强的抗风化能力,能较完好地保存下来,相对花粉等微体植物化石具有抗氧化、比重大、分散程度低、原地埋藏等特点[2]。植硅体抗氧化,能够长时间保存于土壤、沉积物及地层中, 例如Wu et al., 从1.2亿年前辽西热河生物群古鸟化石胃容物中发现被子植物早期分支木兰类叶子的植硅体,首次证实古鸟类叶食性的早期起源和演化[3];从云南曲靖富源地区出土的距今2.5亿年的卷柏化石含植硅体,证实了卷柏植物具有很强的‘硅生物矿化’能力[4];Zhang et al.鉴定了长江中下游沉积物中的水稻植硅体,重建了我国十万年的水稻演化历史,夯实了中国是水稻起源及发源地[5]。植硅体土壤及沉积物保存稳定性,关系古植被、古气候重建的可靠性,关系不同植物植硅体固碳能力评价。不同植物种类植硅体保存能力具有差异,一般来说木本植物土壤及沉积物保存能力不及草本。
棕榈科植物属种子植物门被子植物亚门单子叶植物纲的初生目,是世界热带地区最重要的代表之一[6],其因种类繁多、形态各异、具有其他树种无可媲美的优点,而被世界各地广泛种植和利用。棕榈科植物生产丰富的植硅体,其植硅体主要存在于皮下层细胞外部和栅格细胞叶泡内部,它被认为在植物细胞代谢过程中具有重要的作用[7],可能具有增强植物的光和作用、增强对疾病和虫害的抵抗能力和机械支撑作用[6]。棕榈科植物主要分布在南北半球热带、亚热带,少部分分布于温带温湿地区,环境指示意义明显,能够指示温暖湿润的气候[8]。棕榈科植硅体广泛发现于土壤及沉积物,含量丰富,同禾本科植物一样具有强的植物代表性,是古植被、古环境重建,农作物起源关注的对象。
土壤及沉积物植硅体产量及植被代表性与植物产量及植硅体保存稳定性密切相关。植硅体在棕榈全身广泛存在,被认为主要存在于栅格细胞液泡内部,产量大量粒径从 20 nm 到 1.2 μm 不等的颗粒[9]。对植物死亡分解后,植硅体会被释放到土壤中,经历一系列的风化过程,由于SiO2是植硅体的主要成分,因此它们具有相对可靠的抗分解、抗高温和抗氧化性质[10],但是植硅体在一定程度上也存在着溶解性[11]。植硅体的化学稳定性受植硅体表面积大小、化学组成、温度、pH值、CO2、燃烧活动等的影响。同时,植硅体溶解量随降水的增加而增加,在潮湿环境中植硅体更加活跃,植硅体溶解稳定性很大程度上受到其制约[12];在土壤条件方面,随着土壤可利用水分的增多,植硅体的溶解性也会随之增强[13]。土壤的pH值为3.5~9.8之间时,植硅体均能稳定保存[14]。植硅体在酸性土壤环境如水稻土中保存较好,不易受到侵蚀,相反植硅体的溶解性在碱性土壤(pH>8)中会增强[15],植硅体的溶解速率与pH呈显著正相关[16]。通过对植硅体化学组分的研究发现表面吸附有金属离子(如Al3+)的植硅体的抗分解能力相对较强[17]。此外,植硅体溶解稳定性与火活动密切相关。Cabanes等[18]分析小麦植硅体的稳定性,将马弗炉燃烧植硅体与未燃烧的植硅体进行比较,发现未燃烧和燃烧的新鲜样品和化石样品都表明,加热至500℃会导致植硅体的溶解变快,同时,未燃烧麦穗的植硅体比未燃烧小麦叶、茎中的植硅体略易溶解,而燃烧麦穗和燃烧的叶、茎之间的植硅体溶解度似乎没有差异。Katz等[19]研究称,加热会影响植硅体的溶解度,因为植硅体在焚烧过程中会吸收其直接微环境中的重金属,从而改变其表面化学成分,影响植硅体表面的离子键,改变植硅体的溶解稳定性;同时加热会改变其折射率,这反过来又影响植硅体二氧化硅中水和羟基含量的变化[20]。Li et al., (2024)[21]认为火活动能够使植硅体吸附炭黑,增强其水溶稳定性,有利于植硅体的保存。
植硅体埋藏稳定性可通过土壤植硅体含量与植物产量进行比对分析,Liu等进行了东北森林土壤植硅体保存与植物生物产量的关系研究(Liu et al., 2020)[22];可以进行植硅体溶解速率比较,徐等(2024)[23]对喀斯特地区常见禾本科不同植物进行溶解速率比对研究,发现不同植物种类溶解速率不同;还可以进行植硅体进行埋藏模拟实验,探讨植硅体保存的影响因素 (Koebernick,et al., 2024)[24]。
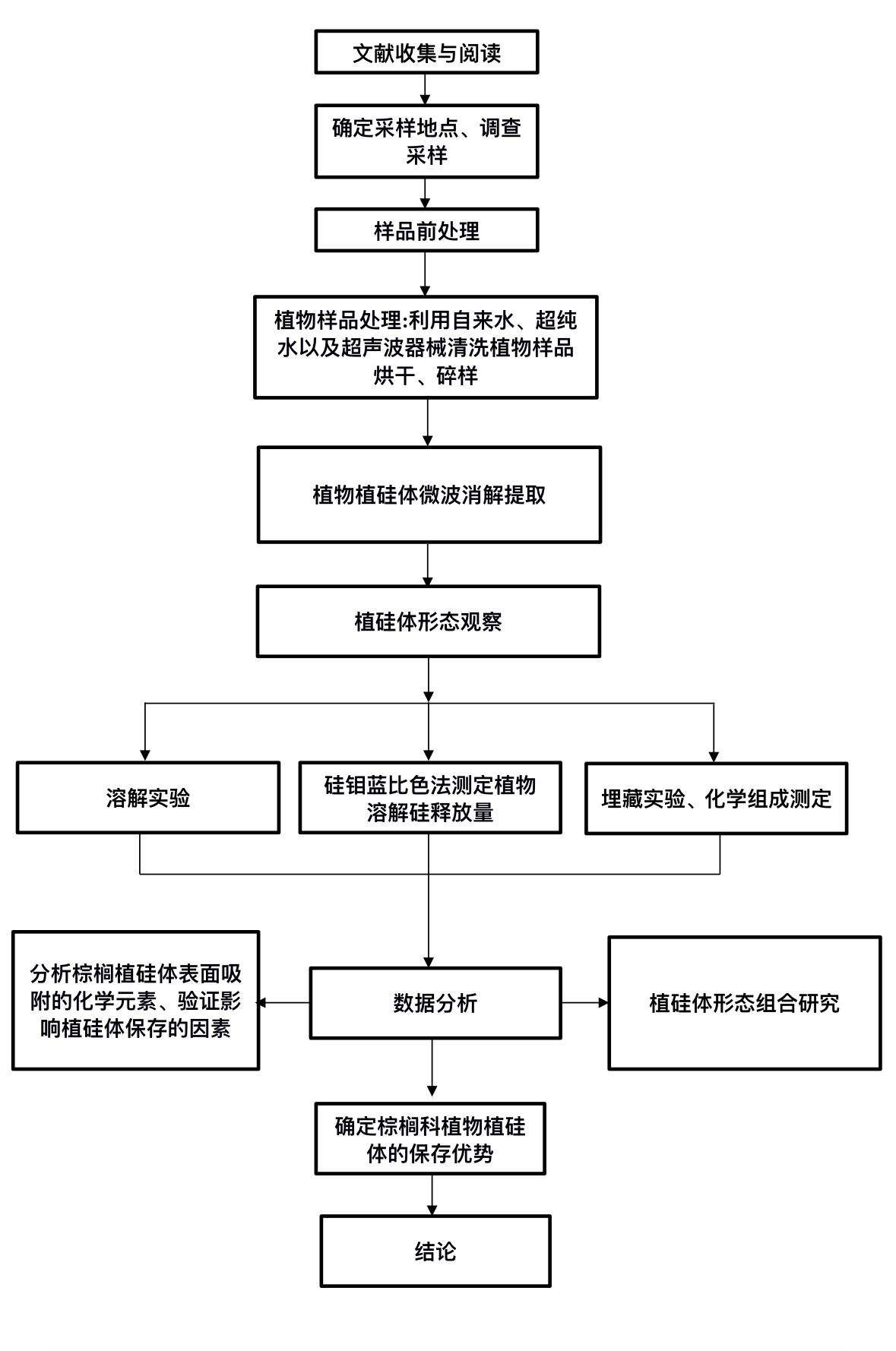
由此可见,目前对植硅体稳定性的研究较为深入,但对不同种类植物对植硅体稳定性的影响暂不清楚;棕榈科植硅体产量丰富,主要形态为刺球型,亚热带植物棕榈植物生物量远低于木本植物,然而棕榈科植硅体具有强代表性,是否与其植硅体具有保存“超”能力有关,其植硅体保存能力受什么因素影响,尚不清楚。本研究对认识土壤及沉积物棕榈科植硅体的鉴定及环境指示具有重要意义,也可为其固碳能力评价提供依据。
参考文献:
[1].王永吉,吕厚远. 植物硅酸体的研究及应用简介[J]. 黄渤海海洋,1989(02):66-68.
[2].王永吉.植物硅酸体研究及应用[M].海洋出版社,1993.
[3].吴妍. 古鸟类叶食性的起源-来自白垩纪木兰类植硅体的新证据[J]. 自然-通讯, 2023.
[4].Zhuo Feng, Qun Sui, Hai-Bo Wei, Jianbo Chen, 二叠纪石松植物中二氧化硅生物矿化的化石证据,《国家科学评论》,第 11 卷,第 12 期,2024 年 12 月,nwae368.
[5].张健平,蒋乐平,于禄鹏,郇秀佳,周力平,王昌盛,靳建辉,左昕昕,吴乃琴,赵志军,孙瀚龙,于炤元,张国萍,朱江平,吴振雷,董亚杰,范宝硕,沈才明,吕厚远. Rice’s trajectory from wild to domesticated in East Asia[J]. Science,2024.
[6].林秀香,陈振东.我国棕榈科植物的研究进展[J].热带作物学报, 2007, 28(3):5.
[7].Thorn V C .Data report: Phytoliths within drill core sediments from Sites 1165 & 1166, Leg 188, Prydz Bay, East Antarctica[J].Proceedings of the Ocean Drilling Program: Scientific Results, 2004, 188:1-12.
[8].Simpson, T. L .Silicon and Siliceous Structures in Biological Systems[J].Silicon & Siliceous Structures in Biological Systems, 1981, 216:1310.
[9].Lins, U., Barros, C., da Cunha, M. 等人。棕榈树中硅生物复合材料的结构、形态和组成 Syagrus coronata (Mart.) Becc.原生质体 220, 0089–0096 (2002).
[10].陈念康,介冬梅,高桂在,等. 植硅体元素封存研究进展[J]. 微体古生物学报,2022,39(04):348-360.
[11].Haynes R J. A contemporary overview of silicon availability in agricultural soils[J]. Journal of Plant Nutrition and Soil Science, 2014, 177(6): 831-844.
[12].Yoshida S, Ohnishi Y, Kitagishi K. Histochemistry of silicon in rice plant: III. The presence of cuticle-silica double layer in the epidermal tissue[J]. Soil Science and Plant Nutrition, 1962, 8(2): 1-5.
[13].Parr J F , Sullivan L A .Phytolith occluded carbon and silica variability in wheat cultivars[J].Plant & Soil, 2011, 342(1-2):165-171.
[14].Liu L, Jie D, Liu H, et al. Response of phytoliths in Phragmites australis to environmental factors in northeast China[J]. Ecological Engineering, 2016, 92: 119-131.
[15].Piperno D R. Phytoliths: a comprehensive guide for archaeologists and paleoecologists[M].Rowman Altamira,2006.
[16].Albert R M, Shahack-Gross R, Cabanes D, et al. Phytolith-rich layers from the Late Bronze and Iron Ages at Tel Dor (Israel): mode of formation and archaeological significance[J]. Journal of Archaeological Science, 2008, 35(1): 57-75.
[17].Buonasera T, Damick A, Shoup D. Not up in smoke: Lipid and phytolith evidence for the function of combustion features at CA-ALA-11, a San Francisco Bay area shellmound[J]. Journal of Archaeological Science: Reports, 2023, 51: 104133.
[18].Cabanes D, Weiner S, Shahack-Gross R. Stability of phytoliths in the archaeological record: a dissolution study of modern and fossil phytoliths[J]. Journal of Archaeological Science, 2011, 38(9): 2480-2490.
[19].Katz O, Cabanes D, Weiner S, et al. Rapid phytolith extraction for analysis of phytolith concentrations and assemblages during an excavation: an application at Tell es-Safi/Gath, Israel[J]. Journal of Archaeological Science, 2010, 37(7): 1557-1563.
[20].Elbaum R, Weiner S, Albert R M, et al. Detection of burning of plant materials in the archaeological record by changes in the refractive indices of siliceous phytoliths[J]. Journal of Archaeological Science, 2003, 30(2): 217-226.
[21].Li, Rencheng, et al. "Charred phytoliths absorb black carbon as potential proxies for paleofire." The Holocene, 4 February 2022, doi:10.1177/09596836221074033.
[22].Liu, L.D., Jie, D.M., Liu, H.Y., Gao, G.Z., Li, D.H., Li, N.N., 2020. Translocation and preservationof soil phytoliths in temperate regions and its implications for palaeoenvironment reconstruction.Catena. 195, 104868.
[23].Li, R., Gu, Z., Vachula, R.S. et al. Fire effects on phytolith carbon sequestration. Sci Rep 14, 30009 (2024).
[24].Koebernick, N., Mikutta, R., Kaiser, K., Klotzbücher, A., Nguyen, A.T.Q., Nguyen, M.N., Klotzbücher, T., 2024. Controls on phytolith stability upon exposure in paddy soils. Geoderma 443, 116821.