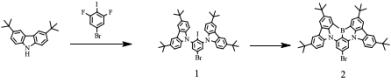
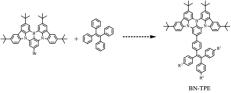
TADF材料的发光机制主要依赖于单重态和三重态激子之间的能量转换,因其“延迟”特性而得名,当TADF材料受到激发后,较低三重态激子通过热活化跃迁到单重激发态的跃迁过程经历了一个通常以数微秒至数百微秒计算的延迟时间,才以荧光的形式发射能量。这种延迟荧光的特性使得TADF材料在OLED领域具有独特的应用价值。其中具有MR骨架的1,4-BN-杂芳烃就是TADF材料的一个经典例子。研究表明,相较于1,2-BN杂芳烃和1,3-BN杂芳烃,1,4-BN杂芳烃表现出优良的芳香性和热化学稳定性(图1)。
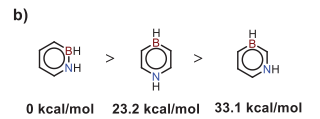
图1 BN杂芳烃热稳定性
根据1,4-BN杂芳烃的形成方式,其合成策略大致可分为以下三种:
(1)过渡金属催化反应:
2017年,Chatani等[1]报道了钯催化制备包埋1,4-BN的蒽(图2),以二卤化物28为主要组成部分,在Pd(OAc)2存在下与二异丙基氨基硼烷29反应,一锅反应生成具有气敏特性的中间体30,中间体30可通过甲醇或NH4Cl水溶液进一步水解,产物31的产率为42%。虽然化合物31的骨架在1961年已经通过亲核取代被报道过,但这是第一个不使用有机锂试剂构建包埋1,4-BN的蒽的例子(图2);
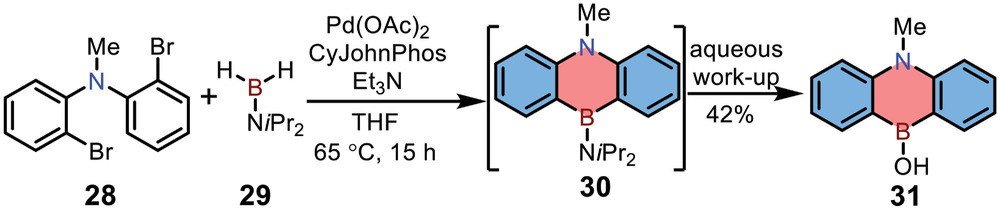
图2钯催化的硼化反应合成包埋1,4-BN的蒽的合成路线
(2)亲核取代反应:
Maitlis于1961年通过亲核取代反应合成了第一个1,4-BN杂蒽,Clark及其同事于1992年[2,3]进一步证实了该骨架的单晶X射线结构。2006年至2010年,Kawashima等人采用相同的合成策略(图3),开发了一系列基于1,4-BN杂蒽的线性衍生物。以1,4-BN杂蒽34为例,首先由2,4-二溴- N -(2,4-二溴苯基)- N -己基苯胺32的Li/Br交换生成中间体33,然后与MesB(OMe)2或TipB(OMe)2一锅反应生成目标化合物。此外,用同样的方法成功地得到了1,4-BN杂蒽衍生物35-38。通过X射线单晶分析确定了化合物36的近共面几何形状,表明化合物36具有良好的π-π共轭骨架结构。其最大吸收与发射波长,与化合物38相比(在608 nm处𝜆abs和625 nm处𝜆em),化合物36的最大吸收和发射波长(在523 nm处𝜆abs, 534 nm处𝜆em)的色移一致。同时,化合物36的大空间位基阻碍了其相互作用,这有利于其高达69%的高光致发光量子产率。
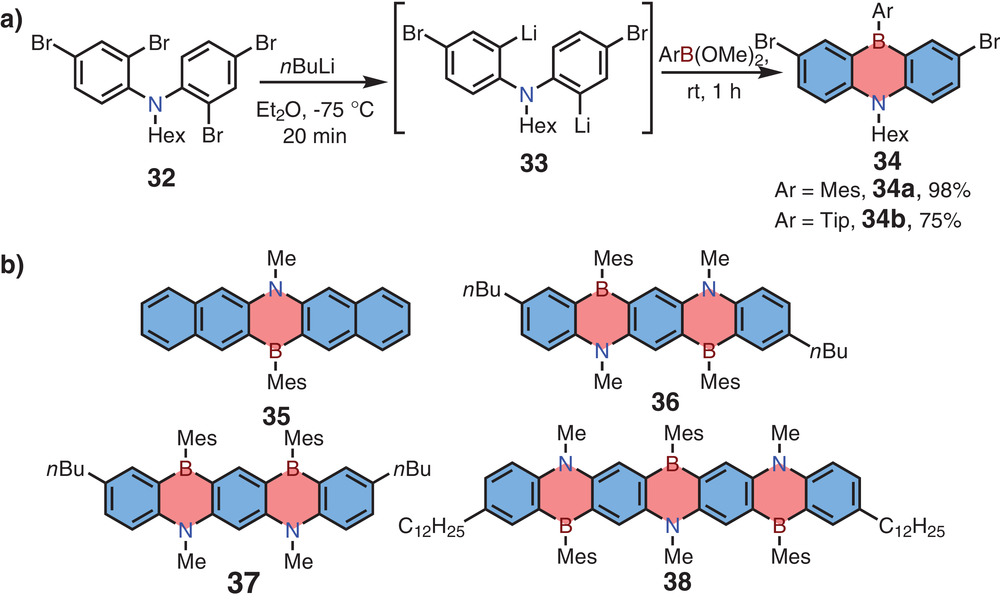
图3 (a)亲核取代反应得到1,4-BN杂蒽;(b)包埋1,4-BN杂蒽的并戊烯和七烯
(3)亲电硼氢化还原反应
亲电硼氢化反应在20世纪50年代首次被报道,并通过这种方法探索了大量结合硼原子的共轭分子。2016年,Hatakeyama等[4]报道了通过亲电硼氢化反应合成N-B-N型1,4-BN杂芳烃59。所得到的化合物在OLED器件中表现出分离的HOMO-LUMO分布,并表现出较窄的发射带(两种化合物的FWHM均为28 nm)。如图4a所示,以1-溴-2,3-二氯苯为原料,通过Buchwald - Hartwig偶联反应制备了中间体58,然后用tBuLi处理58进行Li/Br交换,中间体被BBr3捕获,最后两个C-B键是在叔丁基苯中高温直接C-H硼化形成的,一锅反应得到化合物59。2019年,Zhang和同事[5]报告了用类似的合成策略合成化合物61(图4b)。前体60是由2-溴-1,3,5-三氟苯的亲核取代反应得到的,在硼的对位上具有缺电子单元的化合物61a表现出红移的绿色发射,但由于增强的ICT效应而不影响颜色纯度。
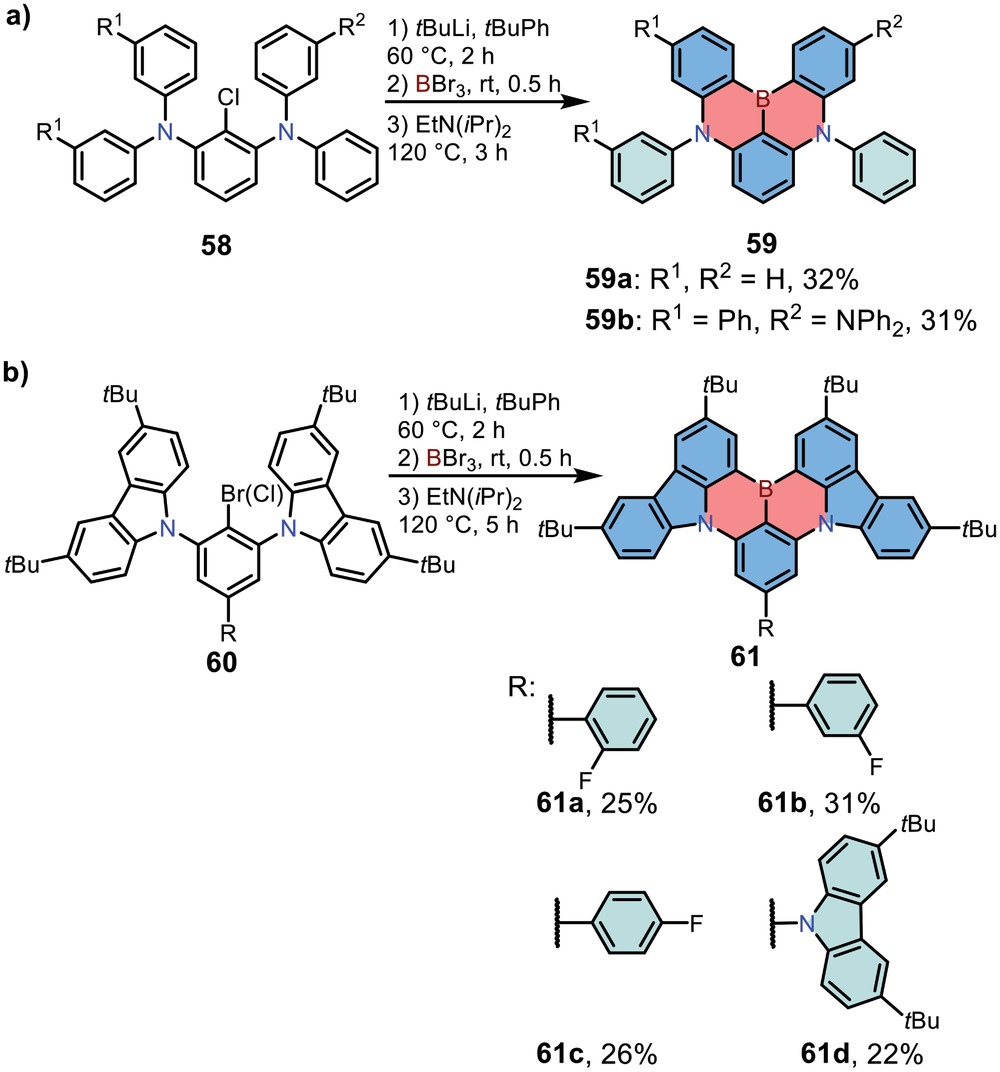
图4 (a、b)亲水性直接C-H硼化反应制备N-B-N型1,4-BN杂芳烃
- T. Igarashi, M. Tobisu, N. Chatani, Angew. Chem., Int. Ed. 2017, 56,2069.
- P. M. Maitlis, J. Chem. Soc. 1961, 425.
- M. Kranz, F. Hampel, T. Clark, J. Chem. Soc., Chem. Commun. 1992,1247
- T. Hatakeyama, K. Shiren, K. Nakajima, S. Nomura, S. Nakatsuka, K.Kinoshita, J. Ni, Y. Ono, T. Ikuta, Adv. Mater. 2016, 28, 2777.
- Y. Zhang, D. Zhang, J. Wei, Z. Liu, Y. Lu, L. Duan, Angew. Chem., Int.Ed. 2019, 58, 16912.

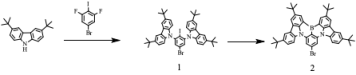
 图1 BN杂芳烃热稳定性
图1 BN杂芳烃热稳定性 图2钯催化的硼化反应合成包埋1,4-BN的蒽的合成路线
图2钯催化的硼化反应合成包埋1,4-BN的蒽的合成路线 图3 (a)亲核取代反应得到1,4-BN杂蒽;(b)包埋1,4-BN杂蒽的并戊烯和七烯
图3 (a)亲核取代反应得到1,4-BN杂蒽;(b)包埋1,4-BN杂蒽的并戊烯和七烯 图4 (a、b)亲水性直接C-H硼化反应制备N-B-N型1,4-BN杂芳烃
图4 (a、b)亲水性直接C-H硼化反应制备N-B-N型1,4-BN杂芳烃